Abstracto
Varios estudios han informado sobre asociaciones entre la vacunación contra la COVID-19 y el riesgo de enfermedades cardíacas, especialmente en jóvenes; sin embargo, el impacto en la mortalidad sigue sin estar claro. Utilizamos datos sanitarios electrónicos nacionales vinculados de Inglaterra para evaluar el impacto de la vacunación contra la COVID-19 y las pruebas positivas de SARS-CoV-2 en el riesgo de mortalidad cardíaca y por todas las causas en jóvenes (de 12 a 29 años) utilizando un diseño de serie de casos autocontrolados. Aquí, demostramos que no hay un aumento significativo de la mortalidad cardíaca o por todas las causas en las 12 semanas posteriores a la vacunación contra la COVID-19 en comparación con más de 12 semanas después de cualquier dosis. Sin embargo, encontramos un aumento de la muerte cardíaca en mujeres después de una primera dosis de vacunas sin ARNm. Una prueba positiva de SARS-CoV-2 se asocia con un aumento de la mortalidad cardíaca y por todas las causas entre las personas vacunadas o no vacunadas en el momento de la prueba.
Otros usuarios están viendo contenido similar
Introducción
El 8 de diciembre de 2020, el Reino Unido (RU) comenzó a administrar vacunas contra la COVID-19 de acuerdo con los grupos prioritarios determinados por el Comité Conjunto de Vacunación e Inmunización (JCVI) 1 . Si bien los ensayos clínicos aleatorizados se centraron en la eficacia a corto plazo contra la infección sintomática, que posteriormente se descubrió que disminuía y se escapaba a las variantes del SARS-CoV-2 2 , 3 , 4 , 5 , 6 , 7 , la evidencia del mundo real ha indicado una efectividad más fuerte y sostenida contra la enfermedad grave y la muerte debido a la COVID-19 6 , 8 , 9 . Sin embargo, también es importante considerar su seguridad, que puede ser difícil de evaluar en ensayos clínicos aleatorizados que no están potenciados para detectar eventos adversos raros 2 , 3 , 10 .
Se han notificado casos raros de eventos adversos graves con las vacunas contra la COVID-19. Estudios previos han demostrado un aumento del riesgo de miocarditis y miopericarditis asociada con las vacunas de ARNm, incluidas BNT162b2 (Pfizer-BioNTech) y mRNA-1273 (Moderna) 8 , 11 , y un mayor riesgo de eventos cardiovasculares trombóticos y otros eventos cardiovasculares raros después de la vacuna ChAdOx1 nCoV-19 (Oxford-AstraZeneca) 12 , 13 . También hay evidencia de una variedad de otras complicaciones neurológicas raras 14 . Sin embargo, el riesgo absoluto de complicaciones graves es bajo y debe evaluarse frente a los mayores riesgos asociados con la infección por SARS-CoV-2 si no se vacuna 15 , 16 . Es particularmente importante determinar el equilibrio entre riesgo y beneficio en personas más jóvenes, debido al menor riesgo de hospitalización y muerte por COVID-19 en este grupo de edad 17 .
Las comparaciones del riesgo de muerte en jóvenes vacunados y no vacunados están sujetas a factores de confusión debido a la priorización de la vacuna y las tasas de vacunación más altas entre aquellos con problemas de salud subyacentes. Para minimizar los posibles factores de confusión, utilizamos un diseño de serie de casos autocontrolados (SCCS), donde cada participante actúa como su propio control, para comparar el riesgo de muerte en las doce semanas posteriores a la vacunación («período de riesgo») con un período de referencia posterior 18 . Con fines de comparación, evaluamos el impacto de una prueba positiva para SARS-CoV-2 en los mismos resultados en individuos vacunados y no vacunados.
En este trabajo, mostramos que, entre la población de Inglaterra de 12 a 29 años, la mortalidad no aumenta significativamente en las primeras doce semanas posteriores a la vacunación contra la COVID-19 en comparación con más de 12 semanas después de cualquier dosis. Las reducciones observadas en la mortalidad por todas las causas son consistentes con un efecto de vacunado sano variable en el tiempo debido al aplazamiento de la vacunación durante períodos de mala salud. Sin embargo, en los análisis de subgrupos encontramos un aumento significativo en el riesgo de muerte cardíaca en mujeres después de una primera dosis de vacunas no ARNm, y un aumento menor y no significativo en la muerte cardíaca después de una segunda dosis de vacunas ARNm en hombres. Por el contrario, una prueba positiva de SARS-CoV-2 se asocia con un aumento de la mortalidad cardíaca y por todas las causas tanto entre las personas vacunadas como entre las no vacunadas.
Resultados
Características de la población de estudio
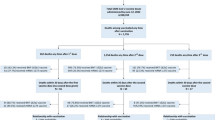
En Inglaterra, se produjeron 3807 muertes de personas de entre 12 y 29 años entre el 8 de diciembre de 2020 y el 25 de mayo de 2022 y se registraron antes del 8 de junio de 2022 (Fig. 1 suplementaria ). De estas, 444 (11,7 %) se debieron a un evento cardíaco y 1512 (39,7 %) estuvieron relacionadas con un registro de vacunación (1510 del NIMS y 2 del extracto complementario del punto de atención del NHS) (Tabla 1 ). El 62,8 % (950) de las primeras dosis, el 51,6 % (505) de las segundas dosis y el 98,8 % (239) de las terceras dosis en el conjunto de datos de registros de defunciones se basaron en ARNm (ya sea la vacuna BNT162b2 de Pfizer-BioNTech o la vacuna mRNA-1273 de Moderna), en lugar de no basadas en ARNm (la vacuna ChAdOx1 de Oxford-AstraZeneca) u otra vacuna o desconocida. De los que recibieron tanto la primera como la segunda vacunación (979), el 11,3 % (111) recibió un tipo diferente de vacuna para cada dosis (Tabla complementaria 1 ). Se incluyen los recuentos de muertes por sexo y vector de la vacuna para las personas que recibieron al menos una dosis de ese vector (Tabla complementaria 2 ).
Entre el 8 de diciembre de 2020 y el 31 de marzo de 2022, se registraron en el HES 1420 muertes hospitalarias entre jóvenes de 12 a 29 años, 630 (44,4 %) de las cuales estaban vinculadas a un registro de vacunación (629 del NIMS y 1 del extracto complementario del punto de atención del NHS). El 63,3 % (399) de las primeras dosis, el 53,5 % (228) de las segundas dosis y el 98,2 % (108) de las terceras dosis en el conjunto de datos de muertes hospitalarias se basaron en ARNm. De los que recibieron tanto la primera como la segunda vacunación (422), el 12,0 % (51) recibió un tipo diferente de vacuna para cada dosis (Tabla complementaria 1 ). Las características de los participantes fueron similares en las tres series de casos (Tabla 1 ).
Los análisis correspondientes de muertes después de una prueba positiva de SARS-CoV-2, entre el 8 de diciembre de 2020 y el 31 de diciembre de 2021, incluyeron 3219 muertes registradas, de las cuales 369 (11,5%) se debieron a un evento cardíaco y 353 (11,0%) estaban relacionadas con una prueba positiva previa de SARS-CoV-2 (297 (9,2%) ocurrieron sin vacunar en la fecha de registro de la prueba y 56 (1,7%) vacunados en la fecha de registro de la prueba). Hubo 1123 muertes hospitalarias correspondientes registradas en HES entre el 8 de diciembre de 2020 y el 31 de diciembre de 2021 de personas que no estaban infectadas al ingresar al hospital, de las cuales 181 (16,1%) estaban relacionadas con una prueba positiva previa de SARS-CoV-2 (150 (13,4%) no vacunados en la fecha de registro de la prueba y 31 (2,8%) vacunados). Las características de los participantes fueron nuevamente similares en las tres series de casos (Tabla 2 ).
En consonancia con una prevalencia creciente de retrasos en el registro debido a la derivación al forense asociada con muertes más recientes, la incidencia observada de muertes registradas en el ONS disminuyó con el tiempo (Fig. 2 suplementaria ). Las muertes hospitalarias registradas en HES no se ven afectadas por los retrasos del forense y no exhibieron esa tendencia. Se observaron patrones similares para los análisis de muertes después de una prueba positiva de SARS-CoV-2 para los conjuntos de datos de muertes registradas y muertes hospitalarias (Fig. 3 suplementaria ).
La figura complementaria 4A muestra el número de muertes cada semana desde la vacunación. Se observó un marcado descenso alrededor de las 12 semanas posteriores a la primera dosis, cuando la mayoría de las personas habrían recibido una segunda dosis. La figura complementaria 4B muestra el número de muertes cada semana desde que se obtuvo un resultado positivo en la prueba del SARS-CoV-2, con un número notablemente mayor de muertes por todas las causas en las primeras 5 semanas.
Incidencia relativa de muerte tras la vacunación contra la COVID-19
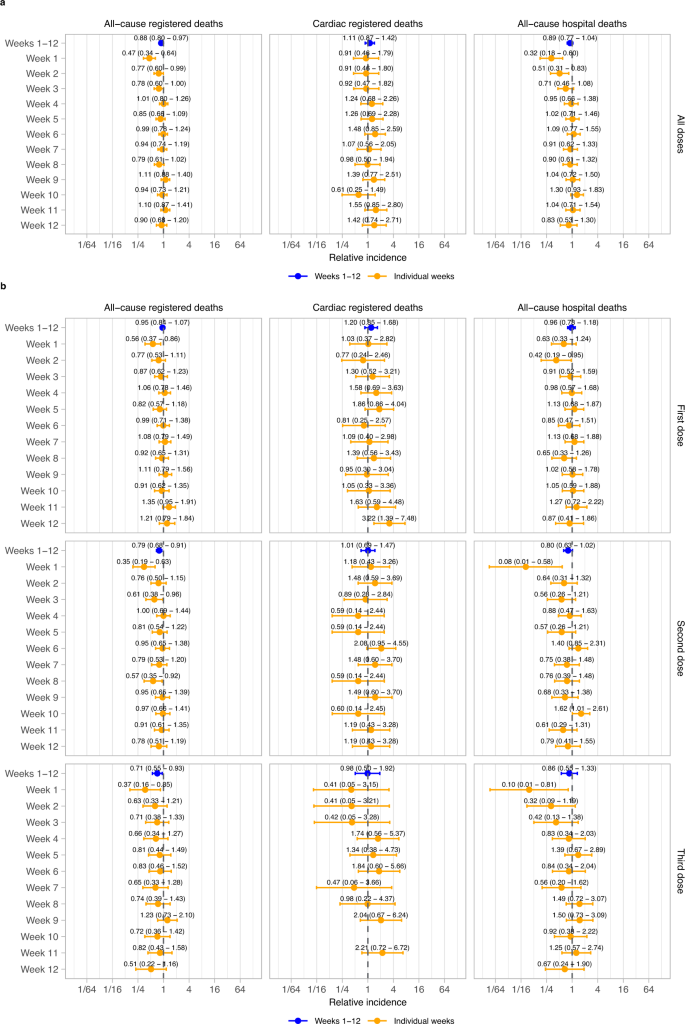
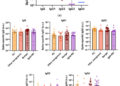
En las doce semanas posteriores a la vacunación, en comparación con los períodos posteriores, no hubo aumentos significativos en la incidencia de ningún resultado de mortalidad para todas las dosis de la vacuna combinadas en cada semana individual o en las doce semanas combinadas (muerte registrada por cualquier causa: razón de la tasa de incidencia, IRR, 0,88, intervalo de confianza del 95%, IC, 0,80, 0,97; muerte cardíaca registrada: IRR 1,11, IC del 95% 0,87, 1,42; muerte hospitalaria por cualquier causa: IRR 0,89, IC del 95% 0,77, 1,04) (Fig. 1a ). Tampoco hubo aumentos significativos en la incidencia de ningún resultado de mortalidad para ninguna dosis individual para las doce semanas combinadas o en cada semana individual en las primeras 12 semanas después de la vacunación, excepto la semana 12 para las muertes cardíacas después de la dosis 1 (IRR 3,22 IC del 95% 1,39, 7,48; Fig. 1b ).
Los datos se presentan como razón de tasas de incidencia con intervalos de confianza del 95 %. Los modelos se ajustan al tiempo calendario; la razón de tasas de incidencia no se muestra si no hay eventos. n = 3807 muertes registradas por todas las causas, 444 muertes registradas por causas cardíacas y 1420 muertes hospitalarias por todas las causas. a Resultados para todas las dosis combinadas. b Resultados por dosis.
Encontramos una disminución significativa en la incidencia de muerte registrada por todas las causas, impulsada por las primeras dos semanas después de la vacunación (cualquier dosis, semana 1: IRR 0,47 [0,34, 0,64]; semana 2: 0,77 [0,60, 0,99]; Fig. 1a ). De manera similar, hubo una disminución del riesgo de muerte hospitalaria en las primeras dos semanas después de la vacunación (cualquier dosis, semana 1: IRR 0,32 [0,18, 0,60]; semana 2: 0,51 [0,31, 0,83]; Fig. 1a ).
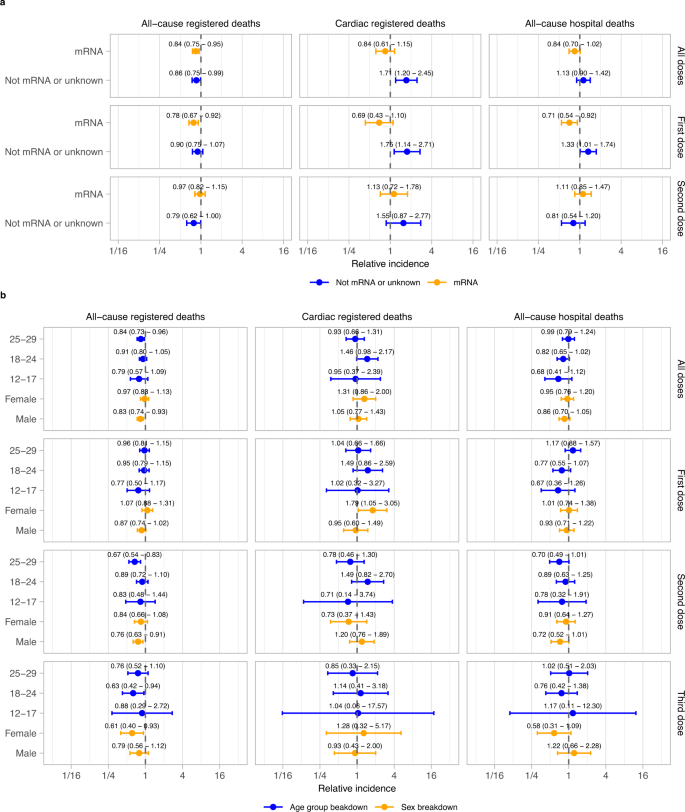
Los análisis de subgrupos por vector de vacuna fueron generalmente consistentes con los resultados principales. Sin embargo, para los vectores de vacuna no ARNm o desconocidos (que consisten principalmente en ChAdOx1 Oxford-AstraZeneca) para la primera dosis y todas las dosis combinadas, hubo aumentos significativos en la incidencia de muerte cardíaca (primera dosis: IRR 1,75 [1,14, 2,71]; todas las dosis: 1,71 [1,20, 2,45]; Fig. 2a ). Se observó un aumento del riesgo de muerte hospitalaria por cualquier causa después de una primera dosis de una vacuna no ARNm (IRR 1,33 [1,01, 1,74]), pero esto no se vio en las muertes registradas por todas las causas (IRR 0,90 [0,75, 1,07]). Los análisis de subgrupos estratificados por grupo de edad y sexo fueron consistentes con los resultados principales excepto después de la primera dosis en mujeres, en las que aumentó la muerte cardíaca (IRR 1,79 [1,05, 3,05]). Esto correspondió a 1 muerte cardíaca adicional registrada por cada 363 419 (IC del 95 % 238 784, 3 272 867) mujeres de 12 a 29 años vacunadas (Fig. 2b ). Sin embargo, no hubo evidencia de un aumento del riesgo en mujeres después de la segunda o tercera dosis (IRR 0,73 [0,37, 1,43] y 1,28 [0,32, 5,17] respectivamente) o cuando se analizaron todas las dosis combinadas (IRR 1,31 [0,86, 2,00]). Además, no hubo evidencia de mortalidad elevada por todas las causas en este subgrupo después de la primera dosis (muerte registrada por todas las causas: IRR 1,07 [0,88, 1,31]; muerte hospitalaria por todas las causas: IRR 1,01 [0,74, 1,38]).
Los datos se presentan como razón de tasas de incidencia con intervalos de confianza del 95 %. Los modelos se ajustan al tiempo calendario. n = 3807 muertes registradas por todas las causas, 444 muertes registradas por causas cardíacas y 1420 muertes hospitalarias por todas las causas. a Desgloses por vector de vacuna b Desgloses por sexo y grupo de edad. No se presentan los resultados de la tercera dosis porque estos se basan casi todos en ARNm.
Los análisis de subgrupos por vector de vacuna desglosados por sexo (Fig. Suplementaria 5 ) mostraron un mayor riesgo de muerte cardíaca en mujeres después de una primera dosis de una vacuna sin ARNm y para todas las dosis combinadas (primera dosis: IRR 3,52 [1,71 – 7,26]; todas las dosis: 3,02 [1,65, 5,53]) pero no después de una primera dosis o cualquier dosis de vacuna de ARNm (primera dosis: IRR 0,87 [0,41 – 1,85]; todas las dosis: 0,76 [0,43, 1,34]). Sin embargo, no se observó un aumento significativo del riesgo de muerte cardíaca en mujeres después de la segunda dosis de una vacuna de ARNm (IRR 0,59 [0,24, 1,44]) y se observó un aumento no significativo después de una primera dosis de una vacuna sin ARNm (1,88 (0,73, 4,87]). Este aumento del riesgo correspondió a 1 muerte cardíaca registrada adicional por cada 16 486 (IC del 95 % 13 688, 28 426) mujeres de 12 a 29 años que recibieron una primera dosis de una vacuna sin ARNm. También se observó un mayor riesgo de muerte hospitalaria por cualquier causa en mujeres después de una primera dosis y después de cualquier dosis de una vacuna sin ARNm (primera dosis: IRR 1,66 [1,10 – 2,51]; cualquier dosis: 1,55 [1,10, 2,18]), sin embargo, esto no se observó en las muertes registradas por todas las causas (primera dosis: IRR 1,13 [0,85, 1,49]; cualquier dosis: 1,09 [0,86, 1,37]).
También hubo una elevación no significativa en la IRR para muerte cardíaca después de una segunda dosis de una vacuna de ARNm en hombres (IRR 1,70 [0,98, 2,97]), que, de ser válida, correspondería a una muerte cardíaca registrada adicional por cada 359.294 (223.043, -) hombres de 12 a 29 años que recibieron una segunda dosis de una vacuna de ARNm. Este resultado fue sensible a la variación del período de riesgo, sin que se observara ningún aumento con un período de riesgo de 6 semanas (IRR 1,15 (0,60, 2,18)). (Fig. 6 suplementaria ).
Incidencia relativa de muerte tras prueba positiva de SARS-CoV-2
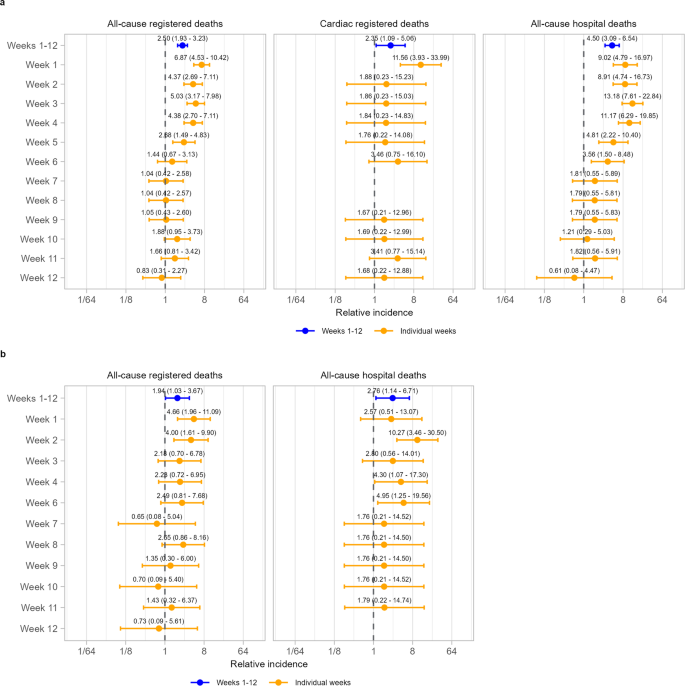
Tras una prueba positiva de SARS-CoV-2 entre personas no vacunadas en la fecha de registro de la prueba, hubo un aumento en la incidencia de muerte cardíaca (IRR para todo el período de 12 semanas: IRR 2,35 [1,09, 5,06]), impulsado por la primera semana (IRR 11,56 [3,93, 33,99]; Fig. 3a ). Durante todo el período de 12 semanas, también se observaron mayores incidencias de mortalidad por todas las causas tanto para las muertes registradas (IRR 2,50 [1,93, 3,23] como para las muertes hospitalarias (IRR 4,50 [3,09, 6,54]), de manera similar más pronunciada en la primera semana (IRR 6,87 [4,53, 10,42] y 9,02 [4,79, 16,97], respectivamente).
Los datos se presentan como razón de tasas de incidencia con intervalos de confianza del 95 %. Los modelos se ajustan al tiempo calendario. n = 3219 muertes registradas por todas las causas, 369 muertes registradas por causas cardíacas y 1123 muertes hospitalarias por todas las causas. a Resultados para personas no vacunadas en el momento de la prueba positiva de SARS-CoV-2. b Resultados para personas vacunadas en el momento de la prueba positiva de SARS-CoV-2. Las muertes cardíacas registradas no se muestran debido a los números pequeños.
También se observó un aumento de la incidencia de muerte por cualquier causa tras una prueba positiva de SARS-CoV-2 entre las personas vacunadas en la fecha de registro de la prueba (IRR 1,94 [1,03, 3,67] para las muertes registradas por cualquier causa; 2,76 [1,14, 6,71] para las muertes hospitalarias por cualquier causa; Fig. 3b ), de manera similar, más pronunciada en las primeras dos semanas. No hubo datos suficientes para analizar las muertes cardíacas entre las personas vacunadas en la fecha de registro de la prueba.
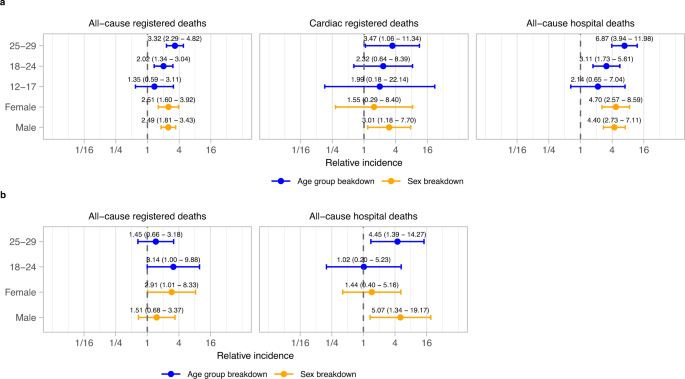
Los aumentos relativos en las tasas de mortalidad después de una prueba positiva de SARS-CoV-2 fueron comparables en todos los subgrupos, pero con mayor incertidumbre en los grupos de edad más jóvenes (Fig. 4 ).
Los datos se presentan como razón de tasas de incidencia con intervalos de confianza del 95 %. Los modelos se ajustan al tiempo calendario. n = 3219 muertes registradas por todas las causas, 369 muertes registradas por causas cardíacas y 1123 muertes hospitalarias por todas las causas. a Resultados para personas no vacunadas en el momento de la prueba positiva de SARS-CoV-2. b Resultados para personas vacunadas en el momento de la prueba positiva de SARS-CoV-2. Las muertes cardíacas registradas no se muestran debido a los números pequeños.
En personas de 12 a 29 años con una prueba positiva de SARS-CoV-2, el mayor riesgo de muerte por cualquier causa registrada en las siguientes doce semanas correspondió a 1 muerte adicional por cada 11.936 (IC del 95 % 10.373, 14.862) personas de 12 a 29 años y no vacunadas en la fecha de registro de la prueba positiva, y 1 muerte adicional por cada 55.661 (37.071, 925.962) personas de 12 a 29 años y vacunadas en la fecha de registro de la prueba positiva.
Análisis de sensibilidad
En los tres análisis de muerte después de la vacunación, las diferentes duraciones definidas del período de riesgo fueron consistentes con los hallazgos principales de permanecer por debajo o no significativamente diferentes de 1 (Fig. Suplementaria 7 ). En los análisis de muertes después de una prueba positiva de SARS-CoV-2 para individuos no vacunados en la fecha de registro de la prueba, las estimaciones de la incidencia relativa de muerte por todas las causas fueron mayores para las definiciones de período de riesgo más corto, en particular para las muertes hospitalarias. Si bien se observó una convergencia hacia uno a medida que aumentaba el período de riesgo definido, no se observó una convergencia completa, y la incidencia relativa pareció estabilizarse por encima de uno para las muertes por todas las causas y cardíacas (Fig. Suplementaria 7A ). En los análisis de muertes después de una prueba positiva de SARS-CoV-2 para individuos vacunados en la fecha de registro de la prueba (Fig. Suplementaria 8B ), las estimaciones de la incidencia relativa de muerte registrada por todas las causas y muerte hospitalaria por todas las causas fueron mayores para las definiciones de período de riesgo más corto y convergieron a 1 a medida que aumentaba el período de riesgo.
Los resultados de los análisis de vacunación y pruebas positivas de SARS-CoV-2 fueron consistentes al ajustar el tiempo del calendario en intervalos quincenales en comparación con el ajuste de spline cúbico restringido de la semana del calendario en el análisis principal (Figs. suplementarias 9 y 10 ). La exclusión de los 23 individuos en el análisis HES de vacunaciones que dieron positivo el día del ingreso hospitalario antes de la muerte proporcionó estimaciones consistentes con el análisis principal (Fig. suplementaria 11 ). La inclusión de las 20 personas en el análisis HES de pruebas positivas de SARS-CoV-2 que dieron positivo el día del ingreso hospitalario antes de la muerte dio estimaciones similares pero ligeramente más altas para las semanas 1 a 12 en comparación con el análisis principal, pero con estimaciones particularmente más altas en la primera semana después de dar positivo (no vacunados en la fecha de la prueba positiva, semanas 1 a 12: IRR 5,01 [3,48, 7,23], semana 1: IRR 15,26 [8,89, 25,95]; vacunados en la fecha de la prueba positiva, semanas 1 a 12 IRR: 2,97 [1,24, 7,12]; semana 1: IRR 3,90 [0,96, 15,86]) (Fig. Suplementaria 12 ).
Discusión
Utilizando un análisis de series de casos autocontrolados en dos fuentes independientes de datos de mortalidad, encontramos evidencia mínima de un aumento de la incidencia de mortalidad cardíaca o por todas las causas en general en las doce semanas posteriores a la vacunación contra la COVID-19 para todos los vectores de vacuna combinados. Sin embargo, encontramos evidencia de un aumento en el riesgo de muerte por todas las causas y cardíaca después de una primera dosis de una vacuna no basada en ARNm entre mujeres, y alguna evidencia de un aumento menor después de una segunda dosis de una vacuna de ARNm en hombres. El aumento después de la primera dosis no se observó en el subgrupo masculino para ninguno de los vectores de vacuna. El subgrupo que recibió vacunas no basadas en ARNm tiene más probabilidades de ser clínicamente vulnerable. La vacuna ChAdOx1 Oxford Astra-Zeneca se retiró para las personas menores de 30 años el 7 de abril de 2021 19 , y hasta el 8 de junio de 2021 la vacunación en este grupo de edad se limitó a los trabajadores de la salud y a las personas que eran clínicamente extremadamente vulnerables. Las personas que eran clínicamente extremadamente vulnerables pueden tener un mayor riesgo de eventos adversos después de la vacunación que la población general. En nuestra población de estudio, el 52% de las personas que recibieron una primera vacuna antes del 7 de abril de 2021 recibieron una vacuna no ARNm o desconocida, en comparación con el 4,3% de las personas que recibieron una primera vacuna el 7 de abril de 2021 o después (Tabla complementaria 3 ). Por el contrario, observamos un aumento del riesgo de mortalidad cardíaca y por todas las causas después de una prueba positiva de SARS-CoV-2 tanto entre las personas no vacunadas como entre las vacunadas. Los resultados fueron sólidos al ampliar la duración del período de riesgo.
Un análisis reciente de datos de Florida (Estados Unidos) encontró un mayor riesgo de muerte cardíaca en las primeras cuatro semanas después de la vacunación con ARNm en personas de 18 a 39 años 20 en comparación con las semanas posteriores. El estudio de Florida utilizó un enfoque de SCCS pero no tuvo en cuenta la exposición múltiple. En cambio, combinaron las muertes después de la primera y la segunda dosis mientras extendían el seguimiento más allá del intervalo entre dosis, lo que introdujo sesgo. De manera similar, excluir a los pacientes en función de cualquier evento posterior a la vacunación (una dosis de refuerzo o una prueba positiva para SARS-CoV-2) también habría sesgado los resultados de la vacunación. Otra distinción entre el estudio basado en EE. UU. y nuestra publicación actual es el tipo de vacunación; En nuestro estudio, la vacunación con ARNm representa principalmente la vacuna BNT162b2 de Pfizer-BioNTech y la vacunación sin ARNm la vacuna ChAdOx1 de Oxford-AstraZeneca, mientras que en los EE. UU., la vacunación con ARNm representa una proporción mayor de la vacuna mRNA-1273 de Moderna y la vacunación sin ARNm representa principalmente la vacuna Ad26.COV2.S de Johnson & Johnson, y que los intervalos de dosificación fueron más cortos en los EE. UU. en comparación con el Reino Unido.
Varios otros estudios han destacado la asociación entre la vacunación contra la COVID-19 y el riesgo de miocarditis y otros eventos cardíacos. La vacunación con vacunas de ARNm se asocia con un mayor riesgo de miocarditis o miopericarditis, especialmente en personas jóvenes, en una investigación que utilizó datos de los EE. UU. 21 , 22 , Dinamarca 11 e Inglaterra 23 , y se encontró un mayor riesgo generalmente entre los hombres jóvenes 24. Encontramos poca evidencia de un mayor riesgo de muerte debido a eventos cardíacos después de una vacuna de ARNm para cualquiera de los sexos. Si bien hubo algunos indicios de un posible aumento del riesgo para los hombres después de una segunda dosis de una vacuna de ARNm, el resultado fue sensible a la elección del período de riesgo.
Si bien las personas vacunadas suelen tener tasas más altas de comorbilidad (y, por lo tanto, mayor mortalidad) en comparación con quienes no están vacunados, con frecuencia se observan estimaciones tempranas de efectos negativos para los resultados de seguridad en estudios que estiman la efectividad de la vacuna, un patrón que es consistente con un efecto en personas vacunadas sanas que varía con el tiempo debido al aplazamiento de la vacunación durante períodos de enfermedad o recuperación 25 .
Nuestros hallazgos de mortalidad cardíaca elevada después de pruebas positivas para SARS-CoV-2 también son consistentes con la evidencia de Suecia, que muestra un riesgo elevado de infarto de miocardio y accidente cerebrovascular isquémico después de COVID-19; 16 sin embargo, los nuestros se basan en uno de los estudios más grandes de mortalidad en una cohorte tan joven, donde las muertes son extremadamente raras.
Si bien el riesgo de mortalidad después de una prueba positiva de SARS-CoV-2 fue más pronunciado en las primeras semanas, nuestros resultados no dejaron claro si el riesgo excesivo se había resuelto por completo a las 12 semanas. Un análisis reciente de cohorte emparejada en una población de mayor edad pero geográficamente similar encontró que el riesgo excesivo de enfermedad cardiovascular se resolvió alrededor de las 12 semanas después de una prueba positiva de SARS-CoV-2 26 .
Nuestro estudio tiene varios puntos fuertes. En primer lugar, utilizamos registros de defunciones y muertes ocurridas en hospitales en toda Inglaterra, vinculados a todos los registros de vacunación, incluidos aquellos que no estaban registrados en la base de datos de vacunación del NIMS porque las personas murieron poco después de la vacunación. Al utilizar una serie de casos autocontrolados, nuestras estimaciones tienen en cuenta las diferencias entre personas, lo que es crucial porque se priorizó la vacunación de los jóvenes que eran clínicamente extremadamente vulnerables.
La principal limitación de nuestro análisis de los datos de registro de defunciones es la demora debida a las derivaciones al forense. No todas las muertes que ocurrieron en el período habían sido registradas. Las muertes de jóvenes tienen más probabilidades de ser derivadas al forense y las demoras en el registro pueden ser sustanciales. El ajuste por el tiempo calendario puede explicar el hecho de que las muertes más recientes tienen más probabilidades de estar bajo investigación forense y, por lo tanto, es menos probable que hayan sido registradas. Pero este ajuste no puede explicar ningún aumento en la derivación al forense relacionado con el tiempo transcurrido desde la vacunación; por ejemplo, si las muertes ocurrieron muy poco después de la vacunación, es más probable que sean investigadas por un forense que las muertes que ocurren en cualquier otro momento. Nuestro análisis utilizando muertes registradas en registros hospitalarios, que no se ven afectados por demoras en el registro, fue consistente con el análisis de muertes registradas, lo que sugiere que la derivación diferencial al forense en el período inmediatamente posterior a la vacunación no afectó sustancialmente al análisis de muertes registradas. Sin embargo, otra limitación del análisis del HES es que no se capturarían las muertes cardíacas súbitas, que habrían ocurrido fuera del hospital.
También podría haberse introducido un sesgo en los análisis de HES debido a las pruebas de rutina para SARS-CoV-2 en el ingreso al hospital 27 . Las pruebas de sensibilidad mostraron que, si bien esto no afecta significativamente los resultados en el análisis principal para las muertes después de la vacunación, las estimaciones de muerte después de una prueba positiva de SARS-CoV-2 están infladas, particularmente en la primera semana, debido a este sesgo. Por lo tanto, las personas cuya prueba positiva de SARS-CoV-2 fue en el ingreso al hospital fueron excluidas del conjunto de datos del hospital para el análisis de pruebas positivas de SARS-CoV-2.
El diseño del SCCS examina la variación del riesgo a lo largo del tiempo en los individuos, por lo que la especificación correcta del período de riesgo es crucial. Nuestros análisis de sensibilidad que exploran diferentes duraciones del período de riesgo fueron todos consistentes con los análisis principales, pero no se habría podido detectar un aumento muy duradero del riesgo después de la vacunación con este enfoque del SCCS. Por el contrario, también es posible que el efecto limitado en el tiempo de la vacuna sana enmascare un aumento más pequeño y a corto plazo del riesgo debido a la vacunación; la miocarditis tiende a aparecer muy pronto después de la vacunación, con evidencia de un tiempo medio desde la vacunación hasta la aparición de los síntomas de 2 días 21 .
Otra implicación del diseño del SCCS es que no se pueden hacer comparaciones entre las diferentes series de casos, como las de los vacunados y los no vacunados en el momento de la prueba positiva del SARS-CoV-2. Se puede esperar que estos grupos difieran en aspectos importantes, como la comorbilidad y la cepa del SARS-CoV-2. Es importante destacar que la diferencia no se puede interpretar como una estimación de la eficacia de la vacuna.
Por último, nuestra capacidad para analizar períodos de riesgo más largos se vio limitada por el espaciamiento entre dosis. Los efectos negativos observados en el análisis de sensibilidad con períodos de riesgo de más de doce semanas sugieren un sesgo negativo con períodos de riesgo que excedían los intervalos de dosificación.
Aunque la vacunación contra la COVID-19 se ha relacionado con un mayor riesgo de miocarditis y otros eventos cardíacos en personas jóvenes, no encontramos evidencia de un aumento sustancial del riesgo de mortalidad, ya sea por eventos cardíacos o en general, a causa de las vacunas de ARNm, lo que sugiere que es poco probable que los casos de miocarditis o miopericarditis debido a las vacunas de ARNm contra la COVID-19 sean fatales. Sin embargo, encontramos evidencia de un mayor riesgo de muerte cardíaca después de una primera dosis de una vacuna sin ARNm entre mujeres. También debe tenerse en cuenta que las vacunas sin ARNm ya no se utilizan en el programa de vacunación del Reino Unido 28 . Esto proporciona la seguridad de que las vacunas de ARNm plantean un riesgo mínimo de aumento de la mortalidad en las primeras doce semanas posteriores a la vacunación en individuos jóvenes. Sin embargo, es importante seguir monitoreando la mortalidad después de la vacunación a medida que se registran más muertes, y ampliar la vigilancia a otros grupos de edad y muertes por otras causas.
Métodos
Se obtuvo la aprobación ética del Comité Asesor de Ética de Datos del Estadístico Nacional (NSDEC(20)12).
Este análisis mejora y amplía un análisis previo publicado por la Oficina de Estadísticas Nacionales 29 , al aplicar un modelo SCCS más apropiado a un conjunto de datos de resultados actualizado, un conjunto de datos de resultados adicional e independiente y análisis de sensibilidad adicionales, como se describe más adelante.
Fuentes de datos
Analizamos por separado dos fuentes independientes de datos sobre muerte: las muertes registradas en la Oficina de Estadísticas Nacionales (ONS) 30 y las muertes hospitalarias registradas en las Estadísticas de Episodios Hospitalarios de Inglaterra (HES) 31 . A diferencia de los registros de defunción, las muertes registradas en HES no están sujetas a retrasos debido a las derivaciones del forense. Los conjuntos de datos de muertes incluyeron las muertes registradas hasta el 8 de junio de 2022 que ocurrieron entre el 8 de diciembre de 2020 (el inicio de la implementación de la vacuna en Inglaterra) y el 25 de mayo de 2022; y los registros de HES donde el estado del alta indicó muertes entre el 8 de diciembre de 2020 y el 31 de marzo de 2022. Cuando se registró la misma muerte tanto en el registro como en los conjuntos de datos del hospital, la fecha de muerte, la fecha de nacimiento y el sexo se tomaron del registro de defunción, de lo contrario se tomaron de HES. Hubo 367 registros de muertes en HES (25,8% del total de 1420) que no tenían un registro de defunción vinculado, probablemente debido a una investigación forense en curso.
Los datos de muerte se vincularon a los datos sobre la vacunación contra la COVID-19 del Servicio Nacional de Gestión de la Inmunización (NIMS) 32 y a un extracto complementario de los datos de atención al paciente del NHS proporcionados por NHS-Digital. Los datos del NIMS incluyen la mayoría de las vacunas contra la COVID-19 administradas en Inglaterra desde el 8 de diciembre de 2020. Sin embargo, en casos excepcionales, si la muerte se registró en el Servicio de datos demográficos personales (PDS) antes de que se enviara el registro de vacunación al NIMS, el registro de vacunación del paciente en el NIMS no se actualiza. El extracto complementario de los datos de atención al paciente del NHS incluye todos los registros de vacunación afectados. Los extractos del NIMS y del punto de atención incluyen todas las vacunaciones registradas hasta el 14 de junio de 2022.
Para evaluar la incidencia relativa de muerte después de una prueba positiva de SARS-CoV-2, vinculamos los registros de defunción con los datos de pruebas nacionales del pilar 1 (pruebas en hospitales) y el pilar 2 (pruebas en la comunidad) 33 registrados entre el 9 de septiembre de 2020 (cuando las pruebas masivas estuvieron disponibles) y el 31 de diciembre de 2021. Estos últimos incluyen tanto la reacción en cadena de la polimerasa de laboratorio como las pruebas rápidas de antígenos autoinformadas.
La vinculación entre bases de datos se realizó utilizando el número NHS, que estaba disponible para el 99,96% de los registros NIMS, el 99,7% de los registros de defunción de ONS, el 99,1% de las muertes en HES y el 100% del extracto del punto de atención de NHS-Digital.
La vinculación y preparación de datos se realizó utilizando R 3.5, Python versión 3.6 y Spark versión 2.4.
Población de estudio
La población del estudio incluyó a todas las personas cuyas muertes se registraron desde el inicio de la campaña de vacunación el 8 de diciembre de 2020 y que tenían entre 12 y 29 años en la fecha de la muerte. No hubo suficientes números ni seguimiento para estudiar la vacunación en niños menores de 12 años. Para el análisis de las muertes después de una prueba positiva de SARS-CoV-2, restringimos aún más la población del estudio a las muertes ocurridas hasta el 31 de diciembre de 2021 (la última fecha en la que se pudo registrar una prueba positiva en nuestro conjunto de datos) y se excluyeron las personas cuya prueba positiva de SARS-CoV-2 fue el día del ingreso al hospital. Dado que el período dominante de Ómicron se define como el que comienza el 20 de diciembre de 2021, los datos cubren principalmente los períodos dominantes de Delta (del 17 de mayo al 19 de diciembre de 2021) y Pre-delta (antes del 16 de mayo de 2021) 34 . Separamos el análisis para las personas que fueron vacunadas o no vacunadas el día en que se registró la prueba positiva de SARS-CoV-2, siendo vacunado el haber recibido al menos una dosis cualquier día antes del día de la infección.
Exposición y resultados
La exposición principal fue cualquier dosis de la vacuna contra la COVID-19 en las doce semanas anteriores. La exposición comparativa fue una prueba positiva de SARS-CoV-2 en las doce semanas anteriores. La fecha de la prueba positiva se define como el inicio del último episodio de COVID-19 para cada individuo, donde un nuevo episodio se definió como un resultado positivo más de 120 días después del inicio de cualquier episodio anterior. Esto está en consonancia con el período de tiempo para la reinfección utilizado en la Encuesta de infección por COVID-19 35 . Los episodios se contaron a partir de la primera prueba positiva, pero solo se incluyeron en el análisis los que ocurrieron el 9 de septiembre de 2020 o después.
Se analizaron tres resultados: muerte por cualquier causa registrada y muerte cardíaca registrada (código I30-I52 de la CIE-10 mencionado en el certificado de defunción), de los registros de defunción de la ONS; y muerte hospitalaria por cualquier causa, registrada en el HES. Cada análisis incluyó a todos los participantes que experimentaron el resultado de interés (casos).
Análisis estadístico
Utilizamos un enfoque SCCS diseñado para manejar múltiples exposiciones dependientes de eventos 36 . La exposición dependiente de eventos ocurre cuando el evento de interés influye en la probabilidad de exposición; la muerte representa un ejemplo extremo en el que cualquier exposición posterior es imposible después del evento. Este enfoque específico de SCCS compara el riesgo de muerte durante un período de riesgo predefinido después de la exposición (vacunación o prueba positiva para SARS-CoV-2) con un período de referencia de todo el tiempo posterior al período de riesgo. Al comparar los períodos de tiempo dentro de los individuos, se controlan implícitamente los factores invariantes en el tiempo, como el sexo y, en general, el grupo de edad y la comorbilidad; los factores que varían en el tiempo se pueden controlar mediante la inclusión de casos no expuestos en el análisis y mediante la inclusión del tiempo del calendario como covariable 37 .
Los participantes fueron seguidos desde el 8 de diciembre de 2020 hasta el 25 de mayo de 2022 para los registros de defunción y el 31 de marzo de 2022 para las muertes en el hospital y no fueron censurados en el momento de la muerte. Para los análisis de la prueba positiva del SARS-CoV-2, el seguimiento finalizó el 31 de diciembre de 2021 cuando finalizaron los datos de la prueba. El período de riesgo se definió como las primeras doce semanas después de la vacunación/prueba positiva, mientras que el período de referencia como todas las semanas posteriores al final del estudio. Además, también se incluyeron todas las semanas anteriores a la vacunación/prueba positiva a partir del 8 de diciembre de 2020, o todas las semanas durante el tiempo de seguimiento si el individuo no estaba vacunado/nunca dio positivo, para ajustar el tiempo del calendario.
La exposición fue la semana desde la vacunación/prueba positiva de SARS-CoV-2 para cada una de las primeras doce semanas individualmente, o las doce semanas juntas. Para la vacunación, las semanas de riesgo se categorizaron además por dosis o se consideraron para todas las dosis combinadas.
Los modelos SCCS se ajustaron utilizando un modelo de regresión de Poisson condicional utilizando un método de pseudoverosimilitud en un conjunto de datos a nivel de persona-semana 36 , 37 , 38 , 39 El día del calendario del inicio de cada semana se incluyó en el modelo utilizando un spline cúbico restringido. El ajuste por tiempo de calendario es una forma de capturar el impacto del aumento de los retrasos en el registro a lo largo del tiempo (es más probable que las muertes más recientes estén bajo revisión forense), así como de las tendencias de mortalidad estacional y las tasas cambiantes de infección por SARS-CoV-2. La duración de cada semana en días se incluyó como una compensación en el modelo, ya que algunas semanas no están completas (como si se produce una vacunación a mitad de una semana). Las razones de tasas de incidencia (IRR) para muertes cardíacas y por todas las causas en períodos de riesgo en relación con los períodos de referencia se estimaron utilizando cada modelo. Se obtuvieron intervalos de confianza del 95% a partir de las estimaciones del modelo. Para las estimaciones principales, también calculamos el 95% de confianza utilizando bootstrap. Se realizaron análisis similares centrándose en individuos no vacunados y vacunados para detectar muertes después de una prueba positiva de SARS-CoV-2.
Cuando la tasa de mortalidad individual fue significativamente diferente de uno, derivamos estimaciones de los efectos absolutos utilizando un método establecido para las series de casos autocontrolados 40 . Utilizamos el número total de personas que dieron positivo en los pilares 1 y 2, estratificado por estado de vacunación en la fecha de registro de la prueba durante el período de interés, como medida de los casos expuestos (Métodos complementarios 1 ).
Todos los análisis se realizaron utilizando R 3.5.
Análisis de subgrupos y de sensibilidad
Los análisis se estratificaron por sexo y grupo de edad (12-17, 18-24, 25-29). Los análisis también se estratificaron por vector de vacuna (ARNm o «no ARNm o desconocido») para las dos primeras dosis. «ARNm» incluye las vacunas Pfizer BNT162b2 Pfizer-BioNTech y mRNA-1273 Moderna. «No ARNm o desconocido» incluye la vacuna ChAdOx1 Oxford-AstraZeneca, todos los demás fabricantes de vacunas registrados y los fabricantes de vacunas no registrados. El análisis de cada vector de vacuna incluyó a todas las personas no vacunadas y a todas las personas que recibieron al menos una dosis del vector de vacuna de interés. Las dosis se renumeraron para corresponder solo a la primera, segunda y tercera dosis del vector de vacuna de interés. También desglosamos el análisis del vector de vacuna por sexo.
Evaluamos la sensibilidad a la especificación del período de riesgo explorando un rango de diferentes duraciones del período de riesgo y al tipo de ajuste del calendario ajustando en intervalos quincenales en lugar de usar un spline cúbico restringido 36 . También evaluamos si los resultados podrían estar sesgados por las pruebas de rutina para la infección por SARS-CoV-2 en el ingreso al hospital al omitir a las personas que tuvieron una fecha de prueba positiva el día del ingreso al hospital para el episodio hospitalario anterior a la muerte en los análisis de muertes hospitalarias.
Participación de los pacientes y del público
Ningún paciente ni miembro del público participó en este estudio.
Resumen del informe
Hay más información sobre el diseño de la investigación disponible en el Resumen del informe de Nature Portfolio vinculado a este artículo.
Disponibilidad de datos
Los datos de origen utilizados en este estudio están sujetos a acceso controlado debido a su naturaleza sensible. La ONS está trabajando para que los datos de registro de defunciones vinculados a los datos de vacunación del Servicio Nacional de Gestión de la Inmunización estén disponibles en el Servicio de Investigación Segura (SRS) de la ONS. Los datos de Test and Trace (no vinculados) también están disponibles a través del SRS, pero actualmente no están vinculados a los datos de registro de defunciones en el SRS. El acceso al SRS está disponible para investigadores acreditados. Los detalles de los requisitos y el proceso de solicitud, y el uso de los datos, están disponibles en ons.gov.uk/aboutus/whatwedo/statistics/requestingstatistics/secureresearchservice. También se puede acceder a los microdatos sobre defunciones y vacunación a través del Servicio de solicitud de acceso a datos digitales del NHS. Los datos de estadísticas de episodios hospitalarios no están disponibles a través de la ONS; estos datos están en poder del NHS England. Todos los datos estadísticos utilizados en este estudio están disponibles en el sitio web de la Oficina de Estadísticas Nacionales.
Disponibilidad del código
El código utilizado en este estudio está disponible en Github 41 .
Referencias
-
Departamento de Salud y Asistencia Social, Comité Conjunto de Vacunación e Inmunización: asesoramiento sobre grupos prioritarios para la vacunación contra la COVID-19, 30 de diciembre de 2020. 2020. [En línea].Disponible: https://www.gov.uk/government/publications/priority-groups-for-coronavirus-covid-19-vaccination-advice-from-the-jcvi-30-december-2020/joint-committee-on-vaccination-and-immunisation-advice-on-priority-groups-for-covid-19-vaccination-30-december-2020 .
-
Polack, FP et al. Seguridad y eficacia de la vacuna de ARNm BNT162b2 contra la COVID-19. N. Engl. J. Med. 383 , 2603–2615 (2020).
-
Baden, LR et al. Eficacia y seguridad de la vacuna contra el SARS-CoV-2 mRNA-1273. N. Engl. J. Med. 384 , 403–416 (2021).
-
Wei, J. et al. Respuestas de anticuerpos y correlaciones de protección en la población general después de dos dosis de las vacunas ChAdOx1 o BNT162b2. Nat. Med. 28 , 1072–1082 (2022).
-
Pérez-Alós, L. et al. Modelado de la disminución de la inmunidad tras la vacunación contra el SARS-CoV-2 y factores que influyen. Nat. Commun. 13 , 1614 (2022).
-
Andrews, N. et al. Eficacia de la vacuna contra la COVID-19 contra la variante ómicron (B.1.1.529). N. Engl. J. Med. 386 , 1532–1546 (2022).
-
Altarawneh, HN et al. Protección contra la variante ómicron de una infección previa por SARS-CoV-2. N. Engl. J. Med. 386 , 1288–1290 (2022).
-
Haas, EJ et al. Impacto y eficacia de la vacuna de ARNm BNT162b2 contra infecciones por SARS-CoV-2 y casos de COVID-19, hospitalizaciones y muertes tras una campaña de vacunación nacional en Israel: un estudio observacional utilizando datos de vigilancia nacional. Lancet 397 , 1819–1829 (2021).
-
Bernal, JL et al. Efectividad de las vacunas Pfizer-BioNTech y Oxford-AstraZeneca sobre los síntomas relacionados con la covid-19, las admisiones hospitalarias y la mortalidad en adultos mayores en Inglaterra: estudio de casos y controles con resultado negativo en la prueba. BMJ 373 , n1088 (2021).
-
Menni, C. et al. Efectos secundarios de la vacuna e infección por SARS-CoV-2 después de la vacunación en usuarios de la aplicación COVID Symptom Study en el Reino Unido: un estudio observacional prospectivo. Lancet Infect. Dis. 21 , 939–949 (2021).
-
Husby, A. et al. Vacunación contra el SARS-CoV-2 y miocarditis o miopericarditis: estudio de cohorte basado en la población. BMJ 375 , 1–9 (2021).
-
Hippisley-Cox, J. et al. Riesgo de trombocitopenia y tromboembolia tras la vacunación contra la COVID-19 y la prueba positiva de SARS-CoV-2: estudio de serie de casos autocontrolados. BMJ 374 , n1931 (2021).
-
Simpson, CR et al. Segunda dosis de las vacunas ChAdOx1 y BNT162b2 contra la COVID-19 y eventos trombocitopénicos, tromboembólicos y hemorrágicos en Escocia. Nat. Commun. 13 , 4800 (2022).
-
Patone, M. et al. Complicaciones neurológicas tras la primera dosis de las vacunas contra la COVID-19 y la infección por SARS-CoV-2. Nat. Med. 27 , 2144–2153 (2021).
-
Boehmer, TK et al. Asociación entre COVID-19 y miocarditis utilizando datos administrativos hospitalarios-Estados Unidos. Morbilidad y mortalidad. Wkly. Rep. 70 , 1228–1232 (2021).
-
Katsoularis, I., Fonseca-Rodríguez, O., Farrington, P., Lindmark, K. y Fors, A.-M. Connolly, Riesgo de infarto agudo de miocardio y accidente cerebrovascular isquémico tras la COVID-19 en Suecia: una serie de casos autocontrolados y un estudio de cohorte emparejado. Lancet (Londres, Inglaterra) 398 , 599–607 (2021).
-
Smith, C. et al. Muertes en niños y jóvenes en Inglaterra después de la infección por SARS-CoV-2 durante el primer año de pandemia. Nat. Med. 28 , 185–192 (2022).
-
Petersen, I., Douglas, I. y Whitaker, H. Métodos de series de casos autocontrolados: una alternativa a los diseños de estudios epidemiológicos estándar. BMJ 354 , i4515 (2016).
-
La Agencia de Seguridad Sanitaria del Reino Unido, JCVI, aconseja sobre la vacuna contra la COVID-19 para personas menores de 40 años. [En línea]. Disponible: https://www.gov.uk/government/news/jcvi-advises-on-covid-19-vaccine-for-people-aged-under-40 . [Consultado el 23 de septiembre de 2022].
-
Exploración de la relación entre la mortalidad por todas las causas y la mortalidad relacionada con el corazón después de la COVID-19. 2022. [En línea]. Disponible: https://floridahealthcovid19.gov/wp-content/uploads/2022/10/20221007-guidance-mrna-covid19-vaccines-analysis.pdf . [Consultado el 01 12 2022].
-
Oster, ME et al. Casos de miocarditis notificados tras la vacunación contra la COVID-19 basada en ARNm en EE. UU. desde diciembre de 2020 hasta agosto de 2021. JAMA 327 , 331–340 (2022).
-
Hause, AM et al. Seguridad de la vacuna contra la COVID-19 en adolescentes de 12 a 17 años — Morbilidad y mortalidad. Wkly. Rep. 70 , 5 (2021).
-
Patone, M. et al. Riesgo de miocarditis tras vacunaciones secuenciales contra la COVID-19 por edad y sexo. Circulation 146 , 743–754 (2021).
-
Pillay, J. et al. Incidencia, factores de riesgo, historia natural e hipótesis. BMJ 378 , e069445 (2022).
-
Remschmidt, C., Wichmann, O. y Harder, T. Frecuencia e impacto de la confusión por indicación y sesgo de vacunado sano en estudios observacionales que evalúan la efectividad de la vacuna contra la influenza: una revisión sistemática. BMC Infect. Dis. 15 , 429 (2015).
-
Rezel-Potts, E. et al. Resultados cardiometabólicos hasta 12 meses después de la infección por COVID-19. Un estudio de cohorte emparejado en el Reino Unido. PLOS Med. 19 , e1004052 (2022).
-
Fonseca-Rodríguez, O., Connolly, A.-MF, Katsoularis, I., Lindmark, K. y Farrington, P. Cómo evitar sesgos en estudios de series de casos autocontrolados de la enfermedad por coronavirus 2019. Stat. Med. 40 , 6197–6208 (2021).
-
Agencia de Seguridad Sanitaria del Reino Unido, Guía para la dosis de refuerzo de otoño contra la COVID-19. 28 de septiembre de 2022. [En línea]. Disponible en: https://www.gov.uk/government/publications/covid-19-vaccination-autumn-booster-resources/a-guide-to-the-covid-19-autumn-booster#:~:text=You%20will%20be%20given%20a,made%20by%20Pfizer%20or%20Moderna . [Consultado el 7 de diciembre de 2022].
-
Oficina de Estadísticas Nacionales, Vacunación contra la COVID-19 y mortalidad en jóvenes durante la pandemia de coronavirus. 03 2022. [En línea]. Disponible: https://www.ons.gov.uk/peoplepopulationandcommunity/healthandsocialcare/causesofdeath/articles/covid19vaccinationandmortalityinyoungpeopleduringthecoronaviruspandemic/2022-03-22 .
-
Oficina de Estadísticas Nacionales, Estadísticas de mortalidad en Inglaterra y Gales QMI. 2021. [En línea]. Disponible en: https://www.ons.gov.uk/peoplepopulationandcommunity/birthsdeathsandmarriages/deaths/methodologies/mortalitystatisticsinenglandandwalesqmi .
-
NHS Digital, Estadísticas de episodios hospitalarios (HES). 2022. [En línea]. Disponible en: https://digital.nhs.uk/data-and-information/data-tools-and-services/data-services/hospital-episode-statistics .
-
NHS, Servicio Nacional de Gestión de la Inmunización. 2022. [En línea]. Disponible en: https://www.scwcsu.nhs.uk/services/nhs-immunisation-management-service/ .
-
Agencia de Seguridad Sanitaria del Reino Unido, Estadísticas de pruebas y rastreo del NHS (Inglaterra): metodología. 2022. [En línea]. Disponible en: https://www.gov.uk/government/publications/nhs-test-and-trace-statistics-england-methodology/nhs-test-and-trace-statistics-england-methodology .
-
Oficina Nacional de Estadísticas, Encuesta de infección por coronavirus (COVID-19), características de las personas que dieron positivo en la prueba de COVID-19, Reino Unido: 19 de enero de 2022. [En línea]. Disponible en: https://www.ons.gov.uk/peoplepopulationandcommunity/healthandsocialcare/conditionsanddiseases/bulletins/coronaviruscovid19infectionsurveycharacteristicsofpeopletestingpositiveforcovid19uk/19january2022 . [Consultado el 15 de septiembre de 2022]
-
Oficina de Estadísticas Nacionales y Universidad de Oxford, artículo técnico de la Encuesta de infecciones por coronavirus (COVID-19): análisis de las reinfecciones por COVID-19: junio de 2021. 2021. [En línea]. Disponible en: https://www.ons.gov.uk/peoplepopulationandcommunity/healthandsocialcare/conditionsanddiseases/articles/coronaviruscovid19infectionsurveytechnicalarticleanalysisofreinfectionsofcovid19/june2021#methodology-update .
-
Ghebremichael-Weldeselassie, Y. et al. Un método de series de casos autocontrolados modificado para exposiciones dependientes de eventos y alta mortalidad relacionada con eventos, con aplicación a la seguridad de la vacuna contra la COVID-19. Stat. Med. 10 , 1735–1750 (2022).
-
Whitaker, HJ, Paddy Farrington, C., Spiessens, B. y Musonda, P. Tutorial de bioestadística: el método de series de casos autocontrolados. Stat. Med. 25 , 1768–1797 (2006).
-
Farrington, CP, Whitaker, H. y Hocine, M. Análisis de series de casos para exposiciones posteriores al evento censuradas, perturbadas o restringidas. Biostatistics 10 , 3–16 (2009).
-
P. Farrington, H. Whitaker y Y. Ghebremichael-Weldeselassie, Estudios de series de casos autocontrolados: una guía de modelado con R, Boca Raton: Chapman & Hall/CRC Press, 2018.
-
Wilson, K. y Hawken, S. Estudios de seguridad de fármacos y medidas de efecto utilizando el autocontrol. Farmacoepidemiología de la seguridad de los fármacos. 22 , 108–110 (2013).
-
Oficina de Estadísticas Nacionales, https://doi.org/10.5281/zenodo.7577228 2023. [En línea].